控制适合的条件,将反应2Fe3++2I- 2Fe2++I2设计成如图所示的原电池。下列判断不正确的是
2Fe2++I2设计成如图所示的原电池。下列判断不正确的是 
A.反应开始时,乙中石墨电极上发生氧化反应
B.反应开始时,甲中石墨电极上Fe3+被还原
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl2固定,乙中石墨电极为负极
试卷相关题目
- 1利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来,如废铝罐和碳棒,食盐水等材料制作可用于驱动玩具的电池.上述电池工作时,有关说法正确的是
A.铝罐将逐渐被腐蚀
B.碳棒上发生的反应为:O2+4e-=2O2-
C.碳棒应与玩具电机的负极相连
D.该电池工作一段时间后碳棒的质量会减轻
开始考试点击查看答案 - 2由铜片、锌片和稀硫酸组成的原电池工作时,电解质溶液的pH
A.不变
B.先变小后变大
C.逐渐变大
D.逐渐变小
开始考试点击查看答案 - 3发生原电池的反应通常是放热反应,在理论上可设计成原电池的化学反应的是
A.C(s)+H2O(g)=CO(g)+ H2(g); △H>0
B.Ba(OH)2·8H2O(s)+2NH4Cl(s)= BaCl2(aq)+ 2NH3·H2O(l)+8H2O(l); △H>0
C.CaC2(s)+2H2O(l)→Ca(OH)2(s)+C2H2(g); △H<0
D.CH4(g)+2O2→CO2(g)+2H2O(l); △H<0
开始考试点击查看答案 - 4微型锂碘电池可用植入某些心脏病人体内的心脏起搏器所用的电源。这种电池中的电解质是固体电解质LiI,其中的导电离子是I-。下列有关说法正确的是
A.正极反应:2Li-2e-==2Li+
B.负极反应:I2+2e-=2I-
C.总反应是:2Li+I2=2LiI
D.金属锂作正极
开始考试点击查看答案 - 5将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是

A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大
D.产生气泡的速度甲比乙慢
开始考试点击查看答案 - 6如图所示的装置中,在产生电流时,以下说法不正确的是

A.Fe是负极,C是正极
B.负极反应式为:Fe-3e-=Fe3+
C.内电路中阴离子移向FeCl2溶液
D.电流由石墨电极流向Fe电极
开始考试点击查看答案 - 7理论上,不能设计为原电池的化学反应是
A.


B.


C.
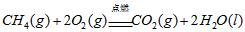

D.
开始考试点击查看答案

- 8用于人造地球卫星的一种高能电池----银锌蓄电池,其电极反应式为:Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-。据此判断氧化银是
A.负极,并被氧化
B.正极,并被还原
C.负极,并被还原
D.正极,并被氧化
开始考试点击查看答案 - 9银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为:2Ag+Zn(OH)2
 Ag2O+Zn+H2O在此电池放电时,负极上发生反应的物质是
Ag2O+Zn+H2O在此电池放电时,负极上发生反应的物质是A.Ag
B.Zn(OH)2
C.Ag2O
D.Zn
开始考试点击查看答案 - 10下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO43-+2I-+2H+
 AsO33-+I2+H2O ”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液。
AsO33-+I2+H2O ”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液。 下列叙述中正确的是
下列叙述中正确的是A.甲组操作时,微安表(G)指针发生偏转
B.甲组操作时,溶液颜色变深
C.乙组操作时,C2做正极
D.乙组操作时,C1上发生的电极反应为I2+2e-=2I-
开始考试点击查看答案
 湘公网安备:43011102000856号
湘公网安备:43011102000856号 
