根据盖斯定律判断右图所示的物质转变过程中,正确的是 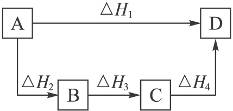
A.ΔH1=ΔH2=ΔH3=ΔH4
B.ΔH1+ΔH2=ΔH3+ΔH4
C.ΔH1+ΔH2+ΔH3=ΔH4
D.ΔH1=ΔH2+ΔH3+ΔH4
试卷相关题目
- 1通过复习总结,你认为下列对化学知识概括合理的是
A.金属离子只有氧化性,非金属离子只有还原性
B.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
C.原子晶体、离子品体、金属晶体、分子晶体中都一定存在化学键
D.在化学反应中,一定有化学键的断裂和形成,并伴有能量的变化
开始考试点击查看答案 - 2下列叙述正确的是:
A.P4和CO2均由共价化合物分子构成
B.CCl4和NH4Cl中均存在共价键
C.Na2O和C60晶体中都不存在单个小分子
D.CH4分子是平面型分子,NH3分子的空间构型为三角锥形
开始考试点击查看答案 - 3下列物质的性质递变规律与化学键无关的是( )
A.还原性:Rb>K>Na>Li
B.沸点:CHI3>CHBr3>CHCl3>CHF3
C.硬度:金刚石>碳化硅>晶体硅
D.稳定性:H2O>H2S>H2Se>H2Te
开始考试点击查看答案 - 4氮化铝(AlN)是一种熔点很高、硬度大、不导电、难溶于水和其他溶剂的晶体。将下列各组物质加热熔化或汽化,所克服粒子间的作用力与AlN克服粒子间的作用力都相同的是
A.水晶,金刚石
B.食盐,硫酸钾
C.碘,硫
D.石墨,硅
开始考试点击查看答案 - 5一带活塞的密闭容器中盛有
A.B组成的混合气体,从状态1自发反应到状态2的变化曲线如下图所示,则该反应过程〔A(g)+B(g)══2C(g)〕是()
 A.放热反应
A.放热反应B.吸热反应
C.对外界没有做功
D.内能不变
开始考试点击查看答案 - 6共价键、离子键、范德华力和氢键是形成晶体的微粒之间的四种作用力。下列晶体:①Na 2O 2②固态氨 ③NaCl ④SiO 2 ⑤冰 ⑥干冰,其中含有三种作用力的是
A.①②③
B.①②⑥
C.②⑤
D.⑤⑥
开始考试点击查看答案 - 7反应
 的能量变化如右图所示。下列说法正确的是
的能量变化如右图所示。下列说法正确的是 
A.12 g C(s)与一定量
 (g)反应生成14 g CO(g),放出的热量为110.5 kJ
(g)反应生成14 g CO(g),放出的热量为110.5 kJB.2 mol C(s)与足量
 (g)反应生成
(g)反应生成 (g),放出的热量大于221 kJ
(g),放出的热量大于221 kJC.该反应的热化学方程式是


D.该反应的反应热等于CO分子中化学键形成时所释放的总能量与
开始考试点击查看答案 分子中化学键断裂时所吸收的总能量的差
分子中化学键断裂时所吸收的总能量的差 - 8家用液化气的主要成分是丙烷、丁烷、丙烯等,将0.112 m 3(标准状况下)丙烷气体完全燃烧,生成二氧化碳气体和液态水,放出11 089 kJ热量,表示上述反应的热化学方程式正确的是
A.C3H8(g)+5O2(g)====3CO2(g)+4H2O(l) ΔH=-11 089 kJ·mol-1
B.C3H8(g)+5O2(g)====3CO2(g)+4H2O(l) ΔH=+2 217.8 kJ·mol-1
C.C3H8(g)+5O2(g)====3CO2(g)+4H2O(l) ΔH=+11 089 kJ·mol-1
D.C3H8(g)+5O2(g)====3CO2(g)+4H2O(l) ΔH=-2 217.8 kJ·mol-1
开始考试点击查看答案 - 9关于化学键的说法正确的是( )
A.化学键是分子与分子之间的作用力
B.形成物质中的化学键时,要吸收能量
C.化学键的断裂和形成是化学反应中能量变化的主要原因
D.形成或断裂同一种化学键,放出或吸收的热量是不相等的,这是化学反应中能量变化的主要原因
开始考试点击查看答案 - 10下列氢键从强到弱的顺序正确的是( ) ①O—H…O ②N—H…N ③F—H…F ④O—H…N
A.①②③④
B.③①④②
C.③②④①
D.③④①②
开始考试点击查看答案
 湘公网安备:43011102000856号
湘公网安备:43011102000856号 
