下列物质的水溶液能发生离子反应的是( )
A.Ba(NO )
) 溶液与NaOH溶液
溶液与NaOH溶液
B.Na CO
CO 溶液与稀硫酸溶液
溶液与稀硫酸溶液
C.稀硫酸溶液与KCl溶液
D.KNO 溶液与Na
溶液与Na SO
SO 溶液
溶液
试卷相关题目
- 1溴化氢气体的热分解温度比碘化氢热分解温度高的原因是( )
A.溴化氢分子中的键长比碘化氢分子中的键长短,键能大
B.溴化氢分子中的键长比碘化氢分子中的键长长,键能小
C.溴化氢分子相对分子质量比碘化氢分子相对分子质量小
D.溴化氢分子间作用力比碘化氢分子间作用力大。
开始考试点击查看答案 - 2下列关于反应类型的判断正确的是( )
A.2Al+2NaOH+2H2O===2NaAlO2+3H2↑ 置换反应
B.FeCl3溶于水发生的反应 复分解反应
C.C2H5OH+HBrC2H5Br+H2O 复分解反应
D.IBr+H2O
开始考试点击查看答案 HBr+HIO 氧化还原反应
HBr+HIO 氧化还原反应 - 3下列各分子中所有原子都满足最外层为8电子结构的是( )
A.N2
B.BF3
C.PCl3
D.HCl
开始考试点击查看答案 - 4已知反应: ①101 kPa时,2C(s)+O 2(g)====2CO(g) ΔH=-221 kJ·mol -1 ②稀溶液中,H +(aq)+OH -(aq) ====H 2O(l) ΔH=-57.3 kJ·mol -1 ③红磷的化学式为P,白磷的化学式为P 4,已知 P 4(s)+5O 2(g)====P 4O 10(s) ΔH=-3 093.2 kJ·mol -1 4P(s)+5O 2(g)====P 4O 10(s) ΔH=-2 954.0 kJ·mol -1 下列结论正确的是
A.由条件可知:红磷转化为白磷是放热反应,所以等质量的红磷能量比白磷低
B.碳的燃烧热大于221 kJ·mol-1
C.稀硫酸与稀NaOH溶液反应的反应热ΔH=-57.3 kJ·mol-1
D.浓硫酸与稀NaOH溶液反应生成1 mol水,放出热量大于57.3 kJ
开始考试点击查看答案 - 5下列有关叙述正确的是
A.因为液态氟化氢中存在氢键,所以其分子比氯化氢更稳定
B.NaHCO3晶体中阳离子和阴离子的个数比为1∶1
C.CO2和SiO2都是共价化合物,两种晶体熔化时克服粒子间作用力类型相同
D.强弱电解质的判断依据是其水溶液导电能力的大小
开始考试点击查看答案 - 6下列说法正确的是( )
A.冰醋酸中醋酸分子之间存在氢键
B.含氢键的物质的熔点一定高于不含氢键的物质
C.碘升华时,分子内共价键不发生变化
D.水结冰体积膨胀与氢键无关
开始考试点击查看答案 - 7氢气在氧气中燃烧时产生明亮的淡蓝色火焰。在反应过程中,破坏1 mol氢气中的H—H键消耗的能量为Q 1 kJ,破坏1 mol氧气中的O—O键消耗的能量为Q 2 kJ,形成1 mol水中的H—O—H键需要的能量为Q 3 kJ。下列关系式正确的是( )
A.2Q1+Q2>Q3
B.2Q1+Q2>2Q3
C.Q1+Q2<Q3
D.2Q1+Q2<2Q3
开始考试点击查看答案 - 8能用键能大小解释的是
A.N2的化学性质比O2稳定
B.常温常压下,溴呈液态,碘呈固态
C.稀有气体一般很难发生化学反应
D.硝酸易挥发而磷酸难挥发
开始考试点击查看答案 - 9下列两组热化学方程式中,有关△ H的比较正确的是( ) ① CH 4g)+2O 2(g) ====CO 2(g)+2H 2O(g);△ H 1 CH 4g)+2O 2(g) ====CO 2(g)+2H 2O(l);△ H 2 ② NaOH(aq) +H 2SO 4(浓)="===" Na 2SO 4(aq) +H 2O(l) ;△ H 3 NaOH(aq) + CH 3COOH (aq)="===" CH 3COONa (aq) +H 2O(l) ;△ H 4
A.△H1>△H2;△H3>△H4
B.△H1>△H2;△H3<△H4
C.△H1=△H2;△H3<△H4
D.△H1<△H2;△H3>△H4
开始考试点击查看答案 - 10试判断下列物质能否溶于水,能溶于水的组合是( ) ①葡萄糖 ②己醛 ③硬脂酸 ④硬脂酸钠 ⑤硬脂酸镁 ⑥乙二酸 ⑦
 ⑧
⑧  ⑨
⑨  ⑩
⑩ 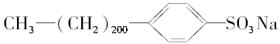
A.①④⑥⑦⑨
B.全溶
C.除⑤⑧外全溶
D.①④⑥⑦
开始考试点击查看答案
 湘公网安备:43011102000856号
湘公网安备:43011102000856号 
