在溶液中有浓度均为0.01mol·L —1的Fe 3+、Cr 3+、Mg 2+等离子,已知: Ksp[Fe(OH) 3]=2.6×10 —39mol 4·L —4;Ksp[Cr(OH) 3]=7.0×10 —31mol 4·L —4 Ksp[Zn(OH) 2]=1.0×10 —17mol 3·L —3;Ksp[Mg(OH) 2]=1.8×10 —11mol 3·L —3 当氢氧化物开始沉淀时,下列哪一种离子所需溶液的pH最小
A.F3+
B.Cr3+
C.Zn2+
D.Mg2+
试卷相关题目
- 1已知氯化银在水中存在沉淀溶解平衡:AgCl
 Ag + + Cl -,25℃时氯化银的 K SP=1.8×10 -10。现将足量的氯化银分别放入下列选项的溶液中,充分搅拌后,相同温度下,银离子浓度最小的是
Ag + + Cl -,25℃时氯化银的 K SP=1.8×10 -10。现将足量的氯化银分别放入下列选项的溶液中,充分搅拌后,相同温度下,银离子浓度最小的是A.100mL蒸馏水中
B.50mL0.1mol?L-1的氯化镁溶液
C.100mL0.1mol?L-1的氯化钠溶液
D.50mL0.1mol?L-1的氯化铝溶液
开始考试点击查看答案 - 2海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
 注:溶液中某种离子的浓度小于
注:溶液中某种离子的浓度小于  ,可认为该离子不存在; 实验过程中,假设溶液体积不变。
,可认为该离子不存在; 实验过程中,假设溶液体积不变。  下列说法正确的是
下列说法正确的是A.沉淀物X为

B.溶液M中存在
 、不存在
、不存在
C.溶液N中存在
 、
、
D.步骤②中若改为加入4.2g NaOH固体,沉淀物Y为
开始考试点击查看答案 和
和 的混合物
的混合物 - 3下列对各种平衡体系的叙述中,完全正确的是一组是 ( ) ①醋酸溶液中存在的电离平衡:CH 3COOH
 CH 3COO -+H +,加水稀释后,溶液中所有离子浓度均减小; ②常温下,在醋酸溶液中加入少量的CH 3COONa固体,会使其电离平衡逆向移动; ③某温度下,容积一定的密闭容器中进行可逆反应:X(g)+Y(g)
CH 3COO -+H +,加水稀释后,溶液中所有离子浓度均减小; ②常温下,在醋酸溶液中加入少量的CH 3COONa固体,会使其电离平衡逆向移动; ③某温度下,容积一定的密闭容器中进行可逆反应:X(g)+Y(g)  2Z(g)+W(s); △H>0平衡后,升高温度,该化学平衡正向移动; ④在上述③的可逆反应中,当容器中气体压强不变时,反应达到平衡; ⑤一定浓度的醋酸钠溶液可使酚酞试液变红,其原因是溶液中存在如下平衡: CH 3COO -+H 2O
2Z(g)+W(s); △H>0平衡后,升高温度,该化学平衡正向移动; ④在上述③的可逆反应中,当容器中气体压强不变时,反应达到平衡; ⑤一定浓度的醋酸钠溶液可使酚酞试液变红,其原因是溶液中存在如下平衡: CH 3COO -+H 2O  CH 3COOH+OH -使得溶液中的c(OH -)>c(H +) ⑥在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,平衡向溶解的方向移动 ⑦在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀
CH 3COOH+OH -使得溶液中的c(OH -)>c(H +) ⑥在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,平衡向溶解的方向移动 ⑦在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀A.①②③④⑤
B.②③④⑤⑥
C.②③⑤⑥⑦
D.①②⑤⑥⑦
开始考试点击查看答案 - 4在重铬酸钾(K 2Cr 2O 7)溶液中存在如下平衡:
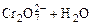



 , 向K 2Cr 2O 7溶液中加入AgNO 3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为
, 向K 2Cr 2O 7溶液中加入AgNO 3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为A.Ag2O
B.Ag2CrO4
C.AgHCrO4
D.Ag2Cr2O7
开始考试点击查看答案 - 5已知常温下反应①、②、③的平衡常数关系为K 1> K 3> K 2,据此所做以下推测合理的是 ①NH 3+H +
 NH 4 +(平衡常数为K 1) ②Ag ++Cl —
NH 4 +(平衡常数为K 1) ②Ag ++Cl —  AgCl(平衡常数为K 2) ③Ag ++2NH 3
AgCl(平衡常数为K 2) ③Ag ++2NH 3  Ag(NH 3) 2 +(平衡常数为K 3)
Ag(NH 3) 2 +(平衡常数为K 3) A.氯化银可溶于氨水
B.银氨溶液中加入少量氯化钠有白色沉淀
C.银氨溶液中加入盐酸无明显现象
D.银氨溶液可在酸性条件下稳定存在
开始考试点击查看答案 - 630℃时等质量的两
 份饱和石灰水,一份冷却到10℃,另一份加入少量氧化钙并保持温度仍是30℃,这两种情况下都不改变的是
份饱和石灰水,一份冷却到10℃,另一份加入少量氧化钙并保持温度仍是30℃,这两种情况下都不改变的是A.溶液的质量
B.氢氧化钙的溶解度
C.溶液中钙离子的数目
D.溶液中钙离子的物质的量浓度
开始考试点击查看答案 - 7在含有浓度均为0.01mol?L -1的Cl -、Br -、I -离子的溶液中,缓慢加入AgNO 3稀溶液,析出三种沉淀的先后顺序是
A.AgCl、AgBr、AgI
B.AgI、AgBr、AgCl
C.AgBr、AgCl、AgI
D.同时析出
开始考试点击查看答案 - 8查阅资料得知Fe 3+、Mg 2+、Al 3+在浓度均为0.1mol·L -1时,氢氧化物沉淀的pH如下表:氢氧化物Fe(OH)3Mg(OH)2Al(OH)3开始沉淀的pH2.310.83.7开始溶解的pH:7.8完全沉淀的pH4.312.45.2完全溶解的pH:10.0 若要从含Fe 3+、Mg 2+、Al 3+的混合溶液中,只得到Fe(OH) 3沉淀,则应调节溶液的pH范围
A.12.4~14
B.7.8~10.0
C.10.0~10.8
D.3.7~5.2
开始考试点击查看答案 - 9常温下, Ksp(CaSO 4)=9×l0 -6,常温下CaSO 4在水中的沉淀溶解平衡曲线如图。下列判断错误的是

A.a、c两点均可以表示常温下CaS04溶于水所形成的饱和溶液
B.a点对应的Ksp不等于c点对应的Ksp
C.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×l0-3mol/L
D.向d点溶液中加入适量CaCl2固体可以变到c点
开始考试点击查看答案 - 10在常温时的下列溶液中,BaSO 4的溶解度最大的是
A.40 mL 1 mol/L的BaCl2溶液
B.30 mL 2 mol/L的Ba(OH)2溶液
C.10 mL纯水
D.50 mL 0.1 mol/L的H2SO4溶液
开始考试点击查看答案
 湘公网安备:43011102000856号
湘公网安备:43011102000856号 
